
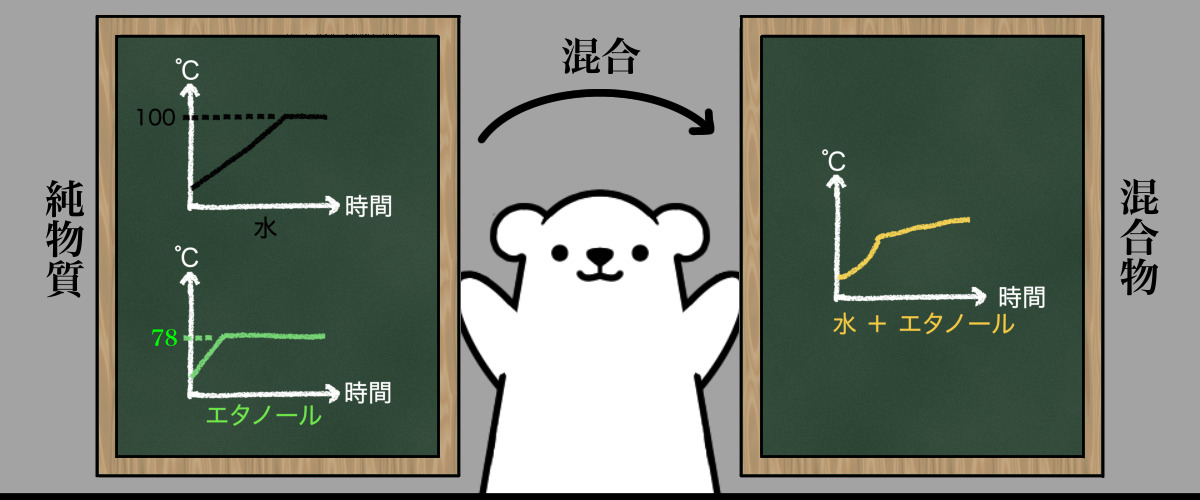
今回は前回の続きで、混合物から純物質を取り出す方法についてです。
混合物から純物質を取り出す方法のことを分離と呼びます。
この分離を繰り返すことで、純物質の純度が上がり精製されていくことになります。
そのため、分離 ≒ 精製となります。

基本的な分離方法は全部で6つあるから紹介していくよ。
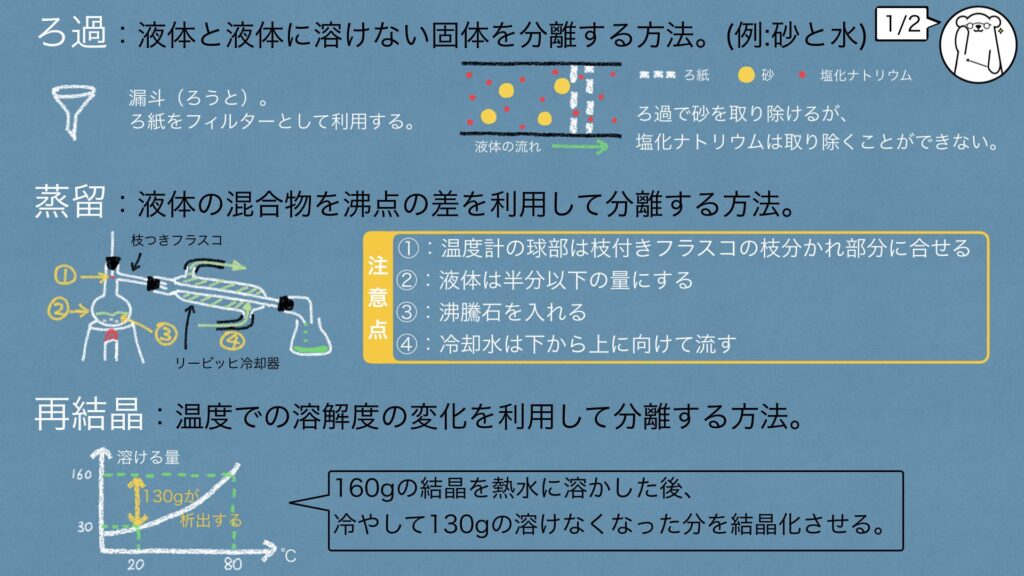
ろ過

液体と固体が混ざっている物に対して行う分離方法がろ過です。
常用漢字ではないので覚える必要はありませんが、正確には「濾過」と書きます。
これは「濾し取る」という意味を持っています。

濾し取る?

簡単に言えば「フィルターを通す」ってことだね。
画像のような水に砂が混ざり、塩化ナトリウムが溶け込んだ液体では、
ろ紙の繊維よりも大きな砂はろ紙を通り抜けることはできません。
そのため、ろ紙の表面には砂がつき、ろ紙を通過した液体(ろ液)は元々の溶液から、
砂が取り除かれた状態になっています。
その一方で、塩化ナトリウムは小さな粒子として液体の中に存在しているので、
ろ過しても取り除くことはできません。

砂が混ざった水みたいなものならキレイに分離できるんだけど、
海水みたいな完全に溶けているものに関しては分離できないんだよ。
あくまでもろ過で分離できるのは、液体に混ざった固体ってことだね。

なるほどね。海水がろ過だけで塩分と水に分けられるなら、
わざわざ淡水化装置なんて機械を使って海水から飲み水を作らなくても済むもんね。
蒸留(分留)

ろ過では分離できない混合物に対してはこの蒸留(分留)を行うことが多いです。
蒸留は「蒸して留める」ことを意味していて、液体を加熱して蒸気にした後に、蒸発したものを冷却して液体に戻す分離方法です。

液体を蒸発させた後に液体に戻すの?
結局何も変わってないんじゃない?
一見無駄に思えるこの操作ですが、この蒸留によって分離できる最大の理由が、それぞれの純物質の持つ沸点の差を利用するからです。
先ほどのろ過で砂が取り除かれたろ液(水と塩化ナトリウム)を分離する際には、この蒸留を行うことで、水のみを取り出すことが可能になります。
これは水の沸点が100℃に対して、塩化ナトリウムの沸点が1413℃なので、加熱した際に蒸発できるのは水だけです。
リービッヒ冷却器を通った先のコニカルビーカーには、最初のろ液よりも水の割合が多い状態で分離することが可能になります。
1つの混合物から2種類以上の物質を蒸留する場合は、得られる物質ごとに「分けながら蒸留する」ので分留と呼ぶこともあります。

分留の代表例は石油の分離だね。
石油は重油、軽油、灯油、ナフサ(ガソリン)と温度ごとに分離され、それぞれの用途に使用されています。
再結晶

3つ目の分離方法が再結晶です。
不純物を含んだ固体から不純物を取り除く分離方法として利用されますが、物質の水に対する溶ける量である溶解度の差を利用しています。
溶解度は温度によって変化し、一般的には温度が高い程、溶解度は増加していきます。

上手くやれば片方だけが溶けて、もう片方は溶けにくい状況を作り出せるんだね
一旦温度を上昇させ、混合物をたくさん溶けしこんだ後に、冷却すること溶けきれなくなった分が一気に純粋な結晶として析出します。

あと、化学物質は同じものが集まろうとする性質があってね。
再結晶で析出した結晶の周りには同じ成分が集まりやすくなるんだ。

あ、それなら知ってる!
凍らせたジュースって味の濃い部分と薄い部分に分かれるのと同じでしょ?

正解だけど、よくそんなの知ってるね
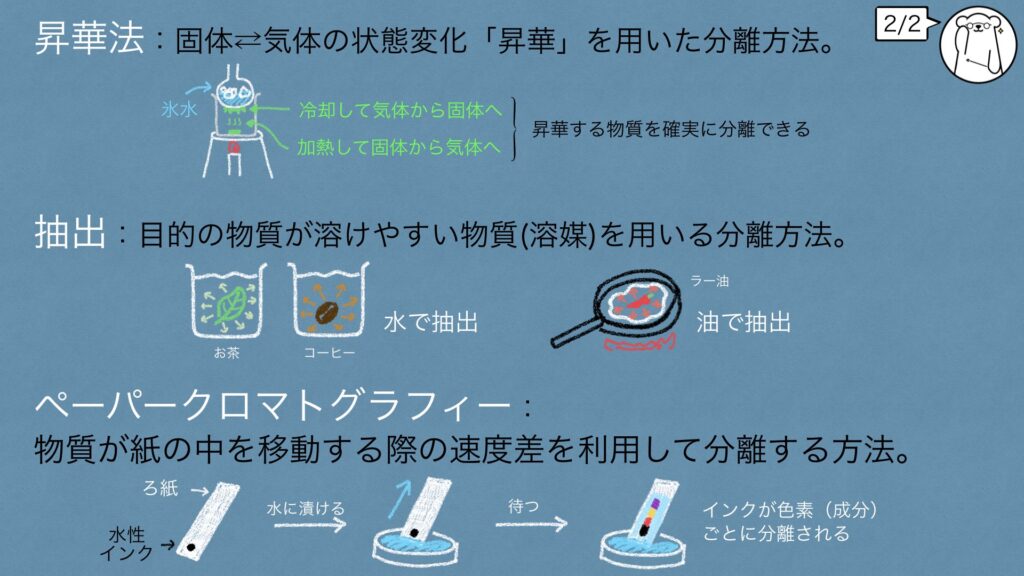
昇華法

次の昇華法も固体を分離する方法ですが、「昇華」という珍しい状態変化を利用します。
普通の物質は固体→液体→気体と固体から気体になる場合は液体になる必要がありますが、この昇華は固体から気体、気体から固体になる状態変化で、液体を飛ばして一気に変化します。
そのため、昇華できない物質と昇華できる物質で簡単に分離することが可能になります。

昇華法って一発で分離ができるんだね!

そうなんだけどね。
それがまともに出来るのがヨウ素くらいしかないんだ。
便利な分離方法の昇華法ですが、唯一の欠点が昇華できる物質がごくわずかであるということです。
ヨウ素やドライアイス(二酸化炭素の固体)の2種が化学基礎で主に扱う昇華ができる物質になります。
ヨウ素の場合は氷水程度の冷却で気体から固体へ昇華させることが可能ですが、二酸化炭素を気体から固体へ昇華させるには−78.5℃に冷却しなければいけません。

防虫剤に使うナフタレンとパラジクロロベンゼンっていう物質も
出来るんだけど、構造が少し難しくて一般的じゃないんだよ。
昇華自体はドライアイスも出来るけど固体に戻すのが大変だから使わないんだ。

ドライアイスって北極の温度よりも低いんでしょ?
そこまで冷やすのはすごく大変そうだね。
抽出

固体中の成分を液体を使って取り出す分離方法が抽出です。
溶け出す物質のことを溶質、溶かし込む媒体となる液体のことを溶媒と呼びます。

身近な例だと、お茶やコーヒーが淹れられるのは抽出をしているからなんだよ。
溶質の種類によって抽出を上手く行うために必要な溶媒と方法が変わってきます。
例えば、緑茶を淹れる場合は熱湯で抽出することが一般的ですが、それは有効成分のカテキンを茶葉から効率良く抽出するために適しているからです。
そのため、苦味や渋味を抑えたい場合は熱湯ではなく水を使って、低温で抽出することで苦味が少なくて甘い緑茶に仕上がるようになります。
水に上手く溶かせない溶質に対しては、油を利用して抽出をします。
具体例としてはラー油が挙げられます。
唐辛子のカプサイシンという辛味成分は水に溶けにくく、油に溶けやすい性質を持っています。
そのため、油で炒めることによって油の中に辛味を閉じ込めることが可能になります。

みんな辛そうにしてるから気になってコッソリ舐めてみたけど、
ほとんど味がしなかったなー。失敗作だったのかな?

鳥類にはカプサイシンが効かないからね。
他にも、筆記用具に使うペンの水性と油性も溶媒の溶媒の違いを表しています。
水性ペンは水に溶けやすいインクを使っており、水をかけるとインクが移るのでにじんでしまいます。
油性ペンの場合は逆に水に溶けにくいインクなので、水をかけてもインクが移れないから滲みません。
その代わりに、油性ペンを落とすときは油系の成分を使わないと落とせないようになっています。

抽出の結果は溶媒の種類だけではなくて、
温度とか他の要素でも変わってくる奥が深いものなんだよ。

「プロの淹れるコーヒーは美味い」ってやつだよね。
そういうのが出来る大人って憧れるよね。
(ペーパー)クロマトグラフィー

最後に紹介するのがクロマトグラフィーです。
紙を使って分離する時はペーパークロマトグラフィー、
気体を使って分離する時はガスクロマトグラフィーのように、
使う媒体によって名前が使い分けることもあります。
これらは物質の中を化学物質が移動する速度の差で分離を行います。

物質って動く速さが違うんだ!?
ペーパークロマトグラフィーだと水性ペンを使うことが多く、紙にインクを付けておいて、水に端を少しだけ浸します。
そうすると、水が紙に染みていくごとにインクも紙の中を移動していき、成分ごとに分離することができます。

そうすると、速い成分は最初のインクの位置よりも遠くにいて、
遅い成分は近い位置に集まってることになるよ!

コメント